24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
背景描述:
某乳腺癌项目012号受试者,基线期血小板计数降低II级,研究者判断有临床意义,并将血小板计数降低记录在病史之中。C2D15周期用药前实验室检查显示恢复了正常水平,然后在C3D1周期用药前又出现血小板计数降低II级。研究者判断血小板计数降低II级记录为AE(如下图),并且在病历中记录该AE与试验药物可能相关。CRC根据病历记录将AE信息录入EDC系统,在某次监查的时候,CRA发现该AE与研究药物相关性在EDC中的数据与化验单上数据不一致。研究者在化验单上评估该AE与试验药物无关,与研究者沟通后,研究者反馈考虑受试者基线有血小板计数降II级,所以判断无关。CRC提出原始记录为与药物可能相关,研究者根据实际情况进行原始资料修改与补充说明,CRC后续也将EDC中的数据做出了修改。
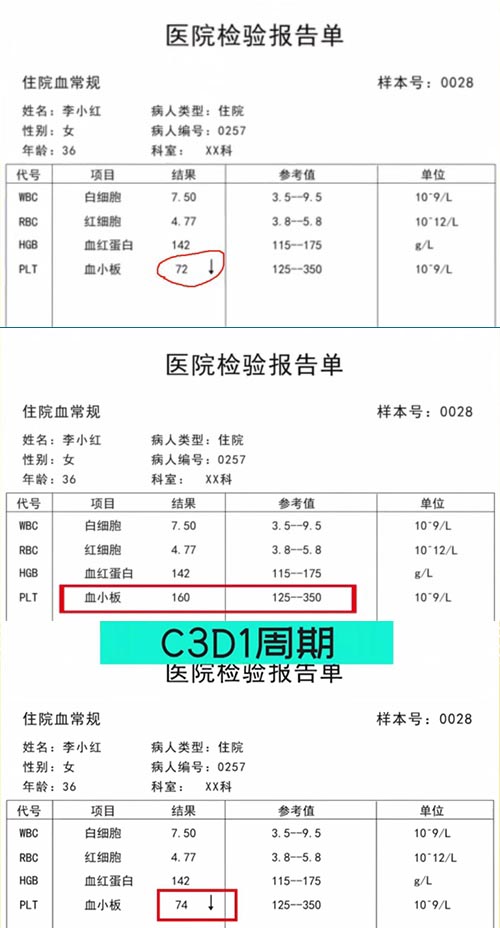
问题发生的根本原因:
1、CRC录入EDC时未进行报告单和原始病历一致性核查;
2、研究者判定AE时前后不一致,未及时更正原始记录。
纠正和预防措施:
1、研究者根据事实情况进行原始资料的补充说明;
2、CRC根据研究者更新后数据进行EDC数据的修改;
3、CRC和研究者确认AE等信息时,首先要提前查阅病史或病历记录,提醒研究者查阅受试者是否有过基线的异常情况,前后逻辑合乎情理;
4、研究者书写病史时,应当保持跟化验单判断或者其他原始文件记录的一致性。当研究者完成病历的书写后,CRC及时对其进行核对,确认无误后在进行EDC数据的录入。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。