24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
与境内外已上市产品相比,采用全新设计、材料或机理,和/或适用于全新适用范围,且对人体具有较高风险的医疗器械,应当经临床试验审批后方可在中国开展临床试验。 上述原则
查看详情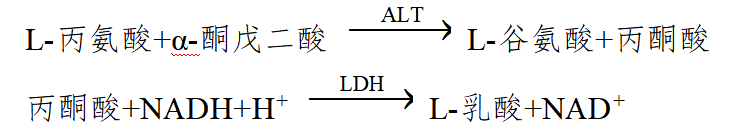
本指导原则旨在指导注册申请人对丙氨酸氨基转移酶(Alanine aminotransferase,ALT)测定试剂注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。
查看详情
本指导原则旨在为医疗器械注册申请人进行卡马西平测定试剂的注册申报提供技术指导,同时也为医疗器械监督管理部门对注册申报资料的审评提供技术参考。 本指导原则是对
查看详情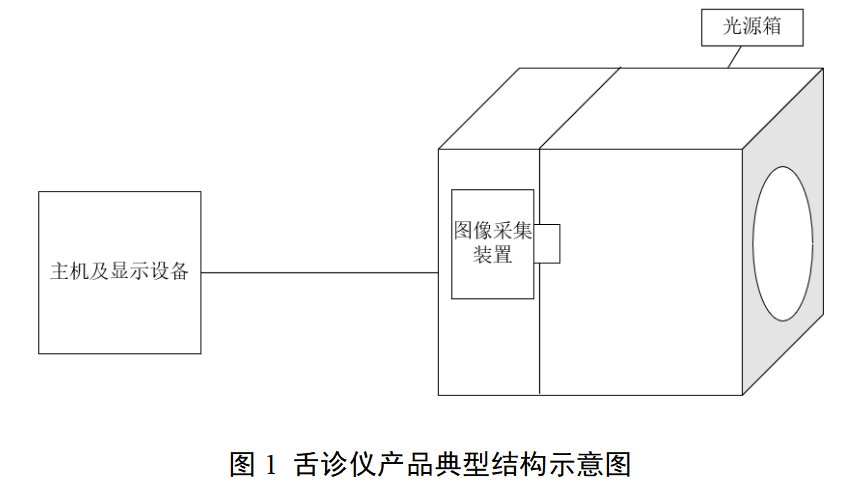
本指导原则旨在指导注册申请人对中医舌诊设备注册申报资料的准备及撰写,同时也为技术审评部门审查注册申报资料提供参考。 本指导原则是对中医舌诊设备的一般要求,申请
查看详情
2026年1月,北京市药品监督管理局共批准注册第二类医疗器械产品37个(具体产品见附件)。 特此公告。 附件:2026年1月批准注册第二类医疗器械产品目录 北京市药品监督管理
查看详情
本指导原则旨在为医疗器械注册申请人进行地高辛检测试剂的注册申报提供技术指导,同时也为医疗器械监督管理部门对注册申报资料的审评提供技术参考。 本指导原则是对该
查看详情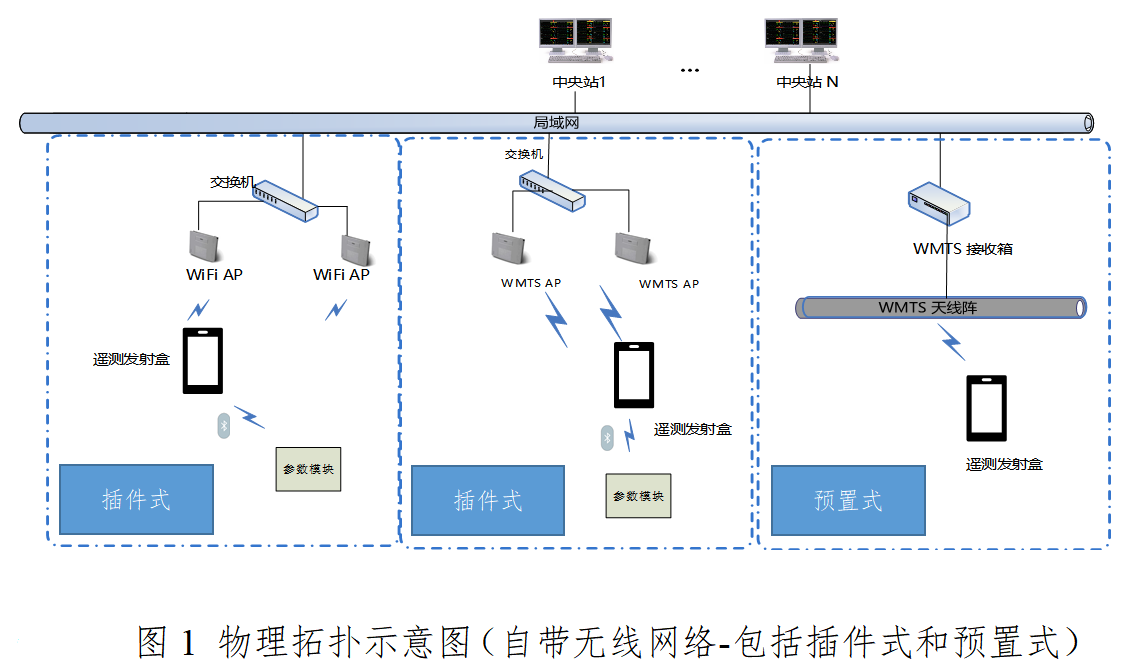
本指导原则旨在指导注册申请人对遥测监护系统注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的审评提供参考。 本指导原则是对用于遥测监护系统产品的
查看详情
本指导原则旨在为医疗器械注册申请人进行丙戊酸测定试剂的注册申报提供技术指导,同时也为医疗器械监督管理部门对注册申报资料的审评提供技术参考。 本指导原则是对该
查看详情