24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

在II/III期无缝临床试验设计当之中,虽然把两个阶段所产生的数据进行合并分析这种方式,能够在相当大的程度上对药物研发的效率起到提升作用,然而与此同时,该方式也会带来一些
查看详情
适应性设计这一被视作创新临床试验方法论的模式,其核心构成是允许研究者在依据试验进程中所积累的各类数据的基础上,按照事先经过严谨讨论与设定的详细计划,对试验方案进行
查看详情
适应性临床试验设计作为一种研究策略而存在,该策略允许依据试验进程里所累积起来的数据情况,按照提前设定好的详细计划,针对试验之中的一个或者多个不同方面展开相应调整,而
查看详情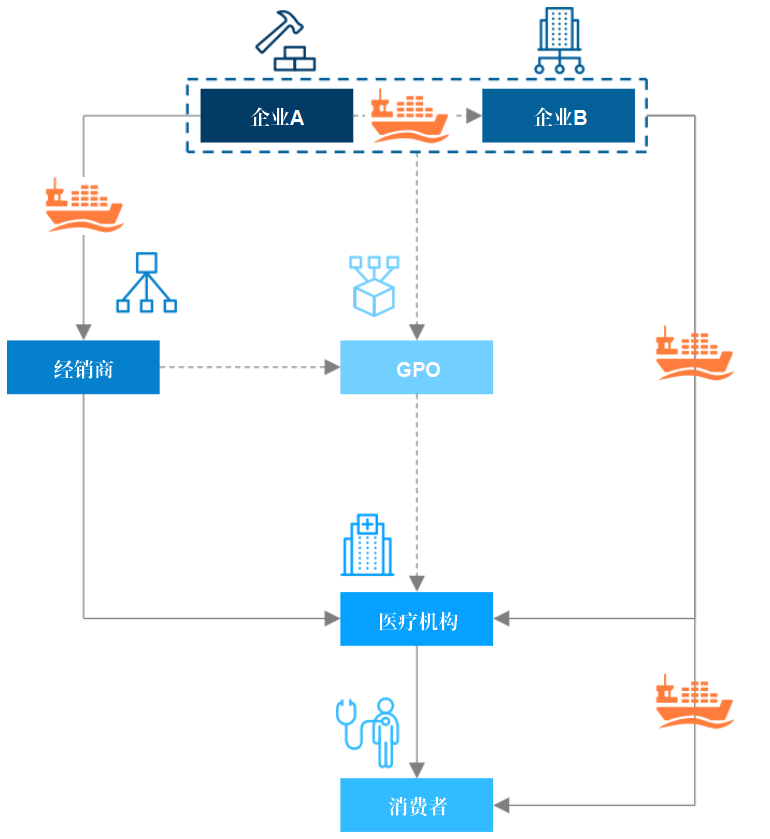
医疗器械全链路覆盖研发制造、流通推广、规模采购等环节,通过技术创新、规模化生产、学术服务、需求整合协同运作,并在全球化布局下形成跨国生态网络,推动产业向健康解决方
查看详情
各有关单位: 按照2026年度指导原则编制计划,我中心现已启动《梅毒螺旋体抗体检测试剂注册审查指导原则》等8项指导原则的制修订工作。现征集制修订工作参与单位,邀请具
查看详情
在多中心临床试验中,实现伦理审查的标准化与互认,是提升新药和新技术研发效率的关键环节。这旨在通过建立协作机制,让一个中心的伦理审查结果能被其他参与中心认可,从而避免
查看详情
临床试验作为新药、新医疗器械上市前验证安全性与有效性的核心环节,其质量与效率直接关系到医学创新成果的转化速度与患者获益。然而,在试验设计、执行和管理的全流程中,常
查看详情
依据国家药品监督管理局与国家卫生健康委员会所联合制定的规定,旨在确保相关机构能够具备开展药物或医疗器械临床试验所需的专业技术水平、组织管理能力以及伦理审查能力
查看详情