24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

医疗器械是保障人类生命健康的不可或缺的工具,而医疗器械的注册则是确保这一工具的安全、有效使用的关键一环。在我国,医疗器械注册分为办理医疗器械注册和医疗器械全包注册两
查看详情
1月18日至19日,2024年全国医疗器械监督管理工作会议在京召开。 会议总结了2023年工作,分析当前形势,并对2024年医疗器械监管工作部署了“以加快推进医疗器械管理法
查看详情
我国首台国产场发射透射电镜发布 由生物岛实验室领衔研制,拥有自主知识产权的首台国产场发射透射电子显微镜于20日在广州发布,将打破国内透射电镜100%依赖进口的局面。
查看详情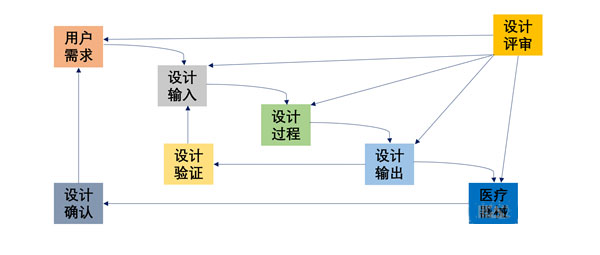
医疗器械的设计开发过程是一个重要而繁琐的环节,其中设计确认是整个过程中不可或缺的一环。设计确认的目标是确保产品能够满足规定的应用要求或预期用途要求,通过提供客观证据
查看详情
近日,乐普医疗(300003)发布公告,宣布公司自主研发的冠脉乳突球囊扩张导管正式获得国家药品监督管理局(NMPA)注册批准,取得Ⅲ类医疗器械注册证,注册证编号:国械注准 202430301
查看详情
2023年,国家药监局共批准注册医疗器械产品2389个。其中,境内第三类医疗器械产品1815个(IVD产品315个),进口第三类医疗器械产品298个(IVD产品23个),进口第二类医疗器械产品25
查看详情
1月22日,国家药监局器审中心发布创新医疗器械特别审查申请审查结果公示(2024年第1号),拟同意7款创新医疗器械项目进入特别审查程序。具体情况如下: 资料来源:CMDE官网1、
查看详情
本指导原则旨在指导注册申请人规范眼科超声乳化和玻璃体切除设备及附件注册申报资料的准备及撰写,同时也为技术审评部门审评注册申报资料提供参考。 本指导原则是对眼
查看详情