24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

本申报属于优先审批项目。依据《医疗器械监督管理条例》(国务院令第739 号)、《体外诊断试剂注册与备案管理办法》(国家市场监督管理 总局令第 48 号)等相关医疗器械法
查看详情
综合评价意见依据《医疗器械监督管理条例》(国务院令第739号)、《体外诊断试剂注册与备案管理办法》(国家市场监督管理总局令第48号)等相关医疗器械法规与配套规章,经对申请人提
查看详情
一、产品概述(一)产品主要组成成分 序号 包装组份 主要成分 规格及数量 1 PCR反应液 阴道毛滴虫 repeatedtarg
查看详情
一、产品概述(一)产品结构及组成 该产品包括非预装人工晶状体(型号:AE2UV)和预装人工晶状体(型号:AE2UL22、AE2UL24、AE2UL28)。预装型号由非预装的AE2UV型人工晶状体和植入
查看详情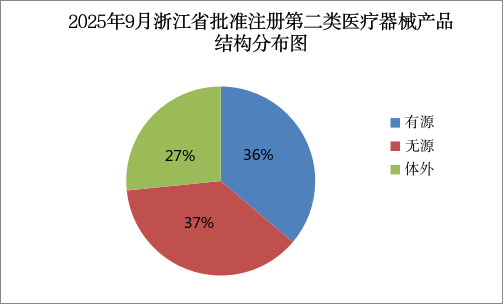
2025年9月,浙江省药品监督管理局共批准注册第二类医疗器械产品94个,其中有源类34个,无源类35个,体外诊断试剂25个(具体产品见附件)。 按照注册申请人所在辖区分析,批准注
查看详情
本指导原则旨在指导注册申请人对登革病毒NS1抗原检测试剂注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的技术审评提供参考。 本指导原则是对登革病
查看详情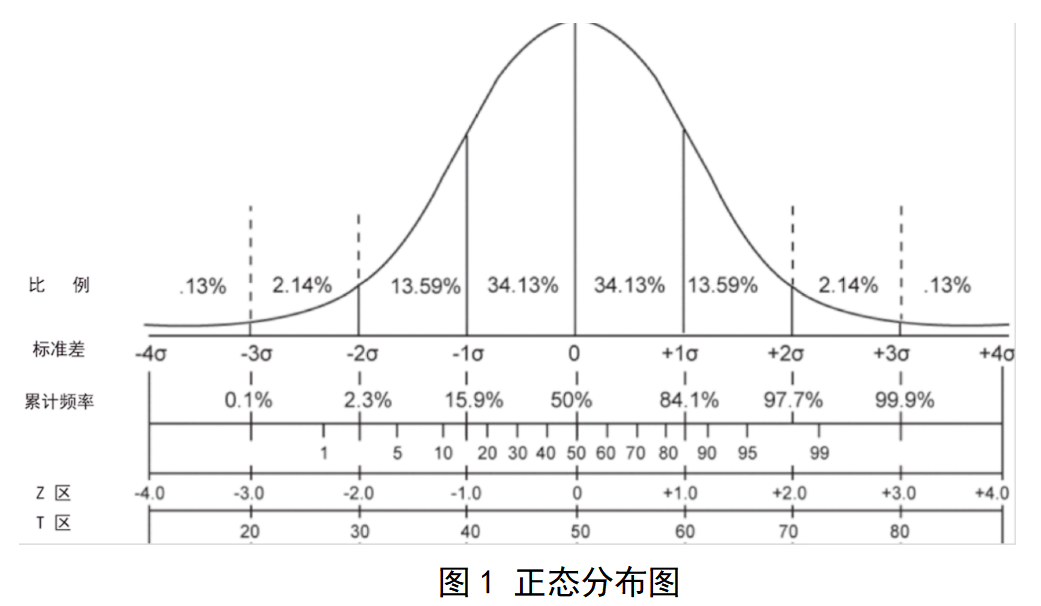
本指导原则旨在指导注册申请人对胎儿染色体非整倍体(T21、T18、T13)检测试剂盒注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的技术审评提供参考。
查看详情
本指导原则旨在指导注册申请人对ABO、RhD血型抗原检测卡(柱凝集法)注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的技术审评提供参考。 本指导原则是
查看详情