24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

于2026年3月4日开幕的全国两会之上,智能医疗器械成为代表委员们热烈讨论的焦点话题,其中涵盖了脑机接口、人工智能辅助诊疗等前沿领域,而政府工作报告中提出的推动创新药和
查看详情
在医疗器械行业于3月3日迎来美敦力与GE医疗这两大巨头联合宣布续签涵盖范围大幅扩展且并非简单续约的多年期全球战略合作协议这一重磅消息的背景下,双方此次合作将美敦力
查看详情
2026年2月进口第一类医疗器械产品备案信息 序号 产品名称 备案号 备案人名称原文 生产地址原文 备案日期 状态 1 足部固定器 国
查看详情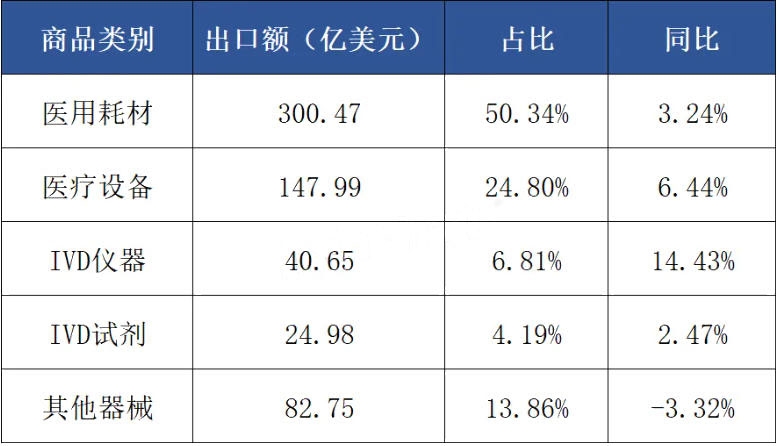
在2026年3月2日由中国医疗器械行业协会所发布的那份关于2025年中国医疗器械出口贸易的统计分析报告之中,有着这样的相关显示,在2025年的时候我国医疗器械出口额达到了596.
查看详情
近日,在市药监局创新审评通道的支持下,第二类创新医疗器械“运动康复系统”顺利获批上市。该产品是北京市2026年获批的首个第二类医疗器械创新产品,截至目前,我市
查看详情
2026年1月,北京市药品监督管理局共批准注册第二类医疗器械产品37个(具体产品见附件)。 特此公告。 附件:2026年1月批准注册第二类医疗器械产品目录 北京市药品监
查看详情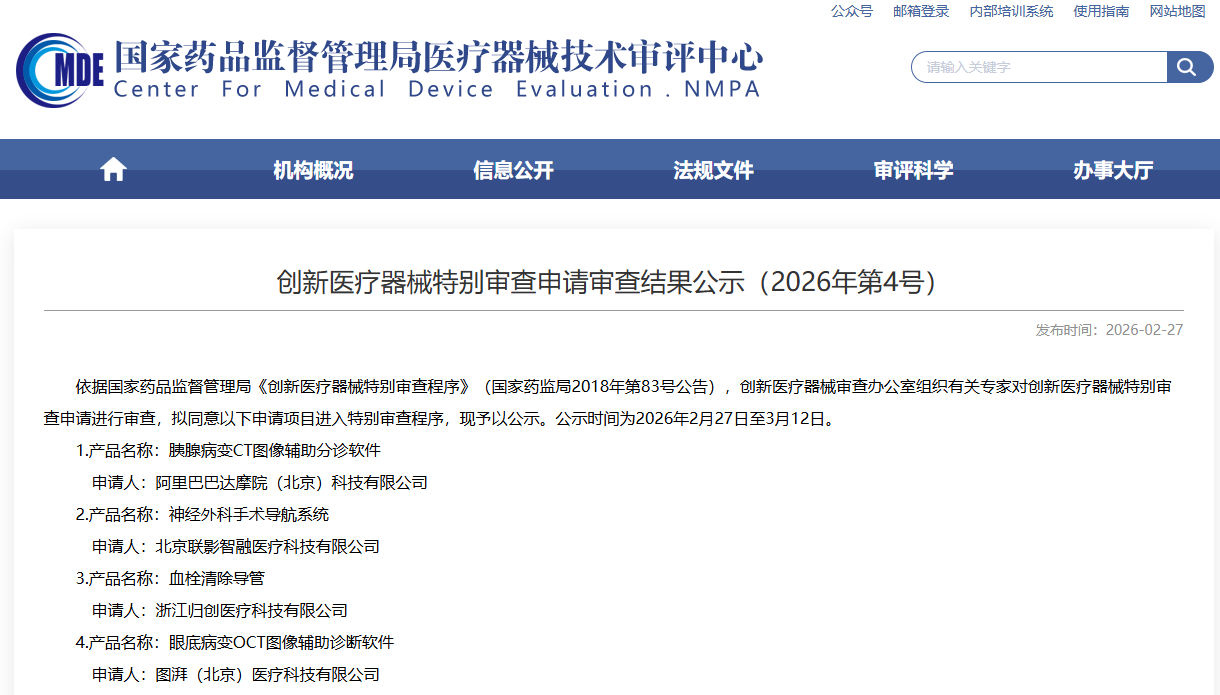
在那由国家药品监督管理局医疗器械技术审评中心所主导的创新医疗器械特别审查申请的相关工作进程之中,有四款在技术创新层面具备显著突破以及临床应用价值的医疗器械产品
查看详情
在2026年初始之际,于医疗器械行业被重磅政策利好所笼罩的大背景之下,江苏、山西、河北、四川等多个省份接连公布了其2026年的重点项目清单,这些清单之中涵盖着数量众多的生
查看详情