24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
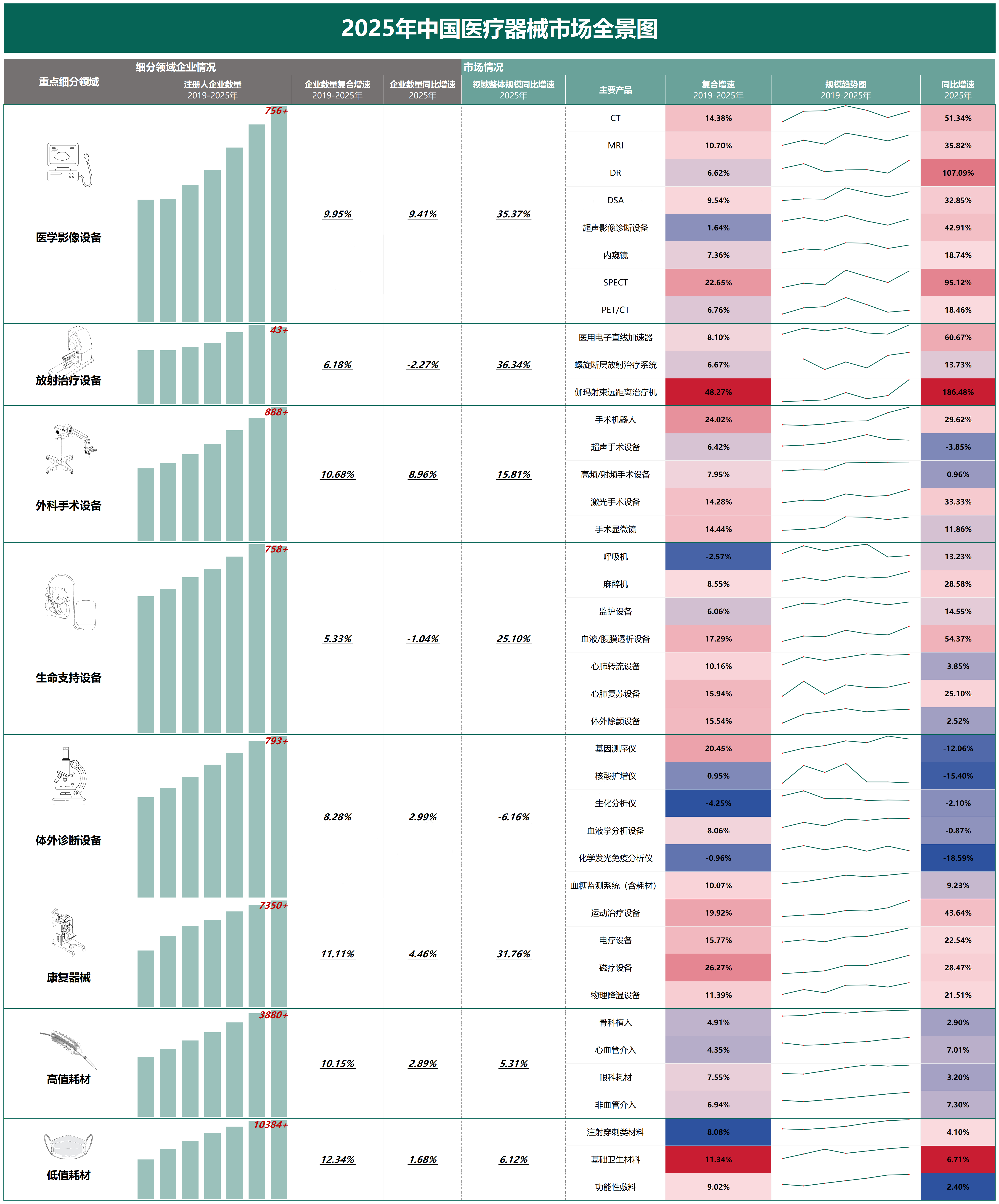
在人口结构逐渐发生变化、技术不断进行迭代以及政策持续给予引导这多重因素的共同驱动之下,2025年的中国医疗器械市场呈现出了一种具有鲜明特点的结构性增长特征,该市场不
查看详情
合肥市新增备案• 文件链接:2025年度新增第一类医疗器械产品目录• 文件内容:包含新增的第一类医疗器械产品信息,以Excel文件形式提供下载。变更备案• 文件链接:20
查看详情
2025年12月,安徽省药品监督管理局共批准首次注册第二类医疗器械产品26个,产品相关信息见附件。 特此公告。 附件:安徽省第二类医疗器械首次注册产品目录(2025年12月)
查看详情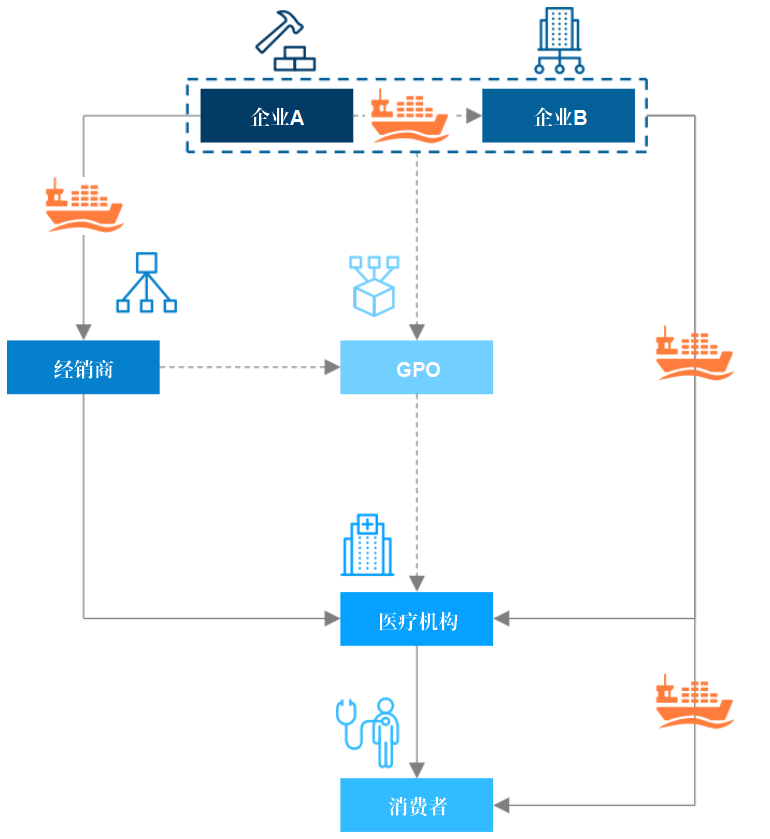
医疗器械全链路覆盖研发制造、流通推广、规模采购等环节,通过技术创新、规模化生产、学术服务、需求整合协同运作,并在全球化布局下形成跨国生态网络,推动产业向健康解决方
查看详情
各有关单位: 按照2026年度指导原则编制计划,我中心现已启动《梅毒螺旋体抗体检测试剂注册审查指导原则》等8项指导原则的制修订工作。现征集制修订工作参与单位,邀请具
查看详情
国家药监局于昨日发布了2025年12月进口第一类医疗器械产品备案信息,本次备案信息涵盖了多个领域的医疗器械产品,包括口腔器械、骨科器械、手术器械、诊断试剂等。 在本
查看详情
2025年12月,河南省药品监督管理局共批准注册第二类医疗器械产品94个,具体产品详见附件。 特此公告。 附件:2025年12月批准注册医疗器械产品目录 2026年1月6日2025
查看详情
2025年12月,广东省药品监督管理局共批准注册第二类医疗器械产品321个,其中首次注册166个,延续注册155个(具体产品见附件)。 特此公告。 附件:2025年12月批准注册第二
查看详情