24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
2025年12月,湖南省药品监督管理局共批准首次注册第二类医疗器械产品89个,新开办生产企业5家(具体产品和企业见附件)。 特此公告。 附件:1.湖南省药品监督管理局2025
查看详情
2025年12月,江西省药品监督管理局共批准注册境内第二类医疗器械产品31个(具体产品见附件)。 特此公告。 附件:2025年12月批准注册医疗器械产品目录.pdf 江西省药
查看详情
2025年12月,江苏省药品监督管理局共批准注册第二类医疗器械产品205个(具体产品见附件)。 特此公告。 附件:2025年12月批准注册第二类医疗器械产品目录、技术审评报
查看详情
2025年12月,浙江省药品监督管理局共批准注册第二类医疗器械产品99个,其中有源类49个,无源类37个,体外诊断试剂13个(具体产品见附件)。 按照注册申请人所在辖区分析,批准
查看详情
2025年12月,国家药监局共批准注册医疗器械产品388个。其中,境内第三类医疗器械产品327个,进口第三类医疗器械产品37个,进口第二类医疗器械产品22个,港澳台医疗器械产品2个(具
查看详情
根据《医疗器械注册与备案管理办法》、《体外诊断试剂注册与备案管理办法》相关规定,2025年12月湖北省药品监督管理局共批准注册医疗器械产品60个。 特此公告。 附
查看详情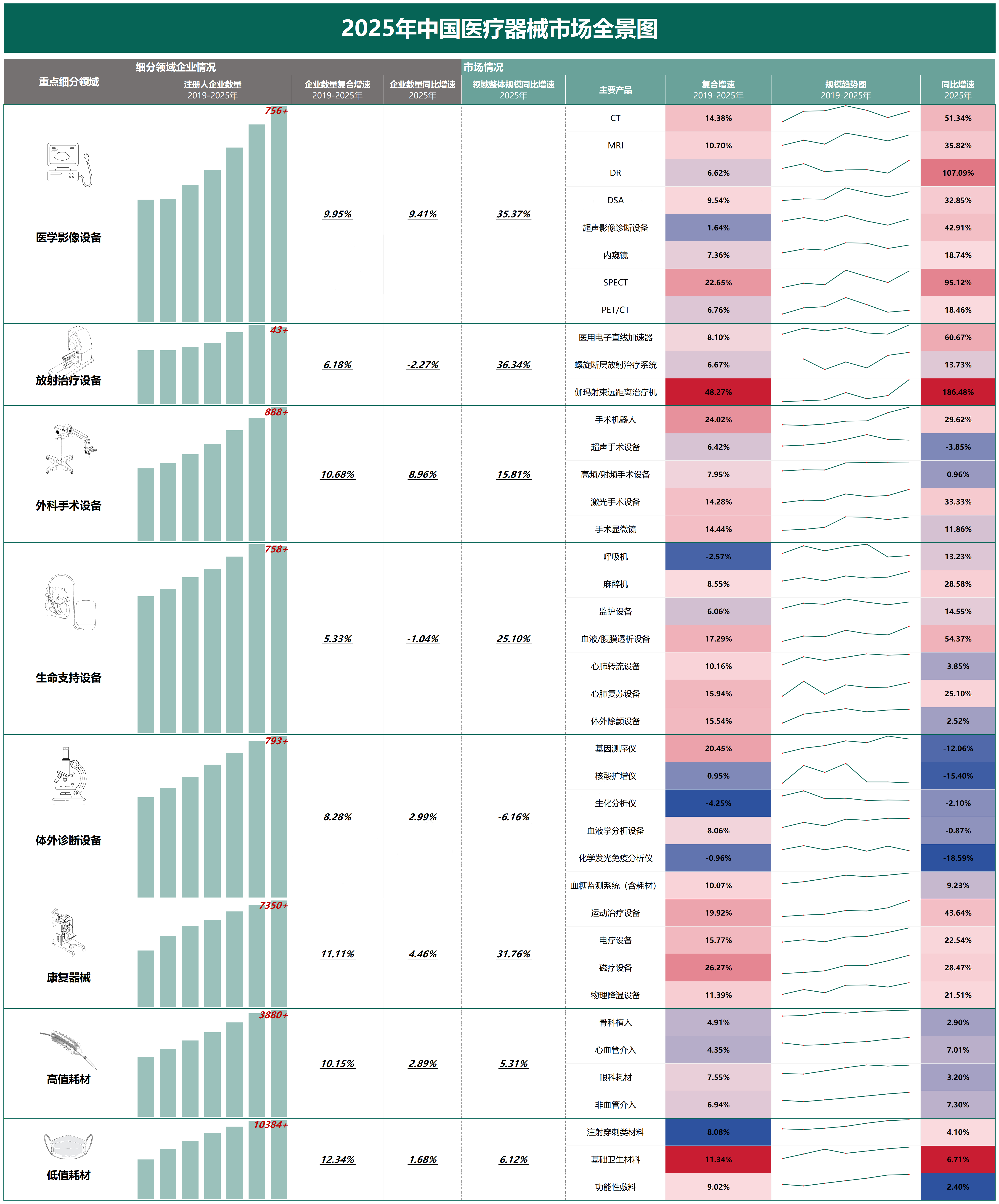
在人口结构逐渐发生变化、技术不断进行迭代以及政策持续给予引导这多重因素的共同驱动之下,2025年的中国医疗器械市场呈现出了一种具有鲜明特点的结构性增长特征,该市场不
查看详情
合肥市新增备案• 文件链接:2025年度新增第一类医疗器械产品目录• 文件内容:包含新增的第一类医疗器械产品信息,以Excel文件形式提供下载。变更备案• 文件链接:20
查看详情