24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
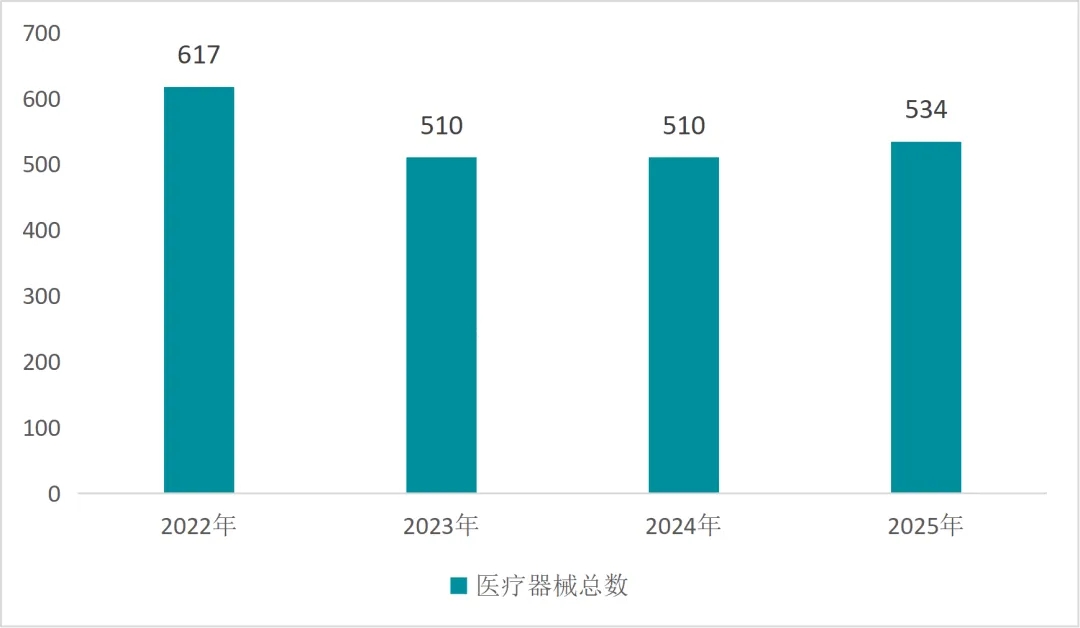
在2025年这个对于中国医疗器械行业而言值得关注的年份里,全年中国医疗器械所获得的FDA认证总量达到534件,该数据相比上一年度呈现出4.7%的微增态势,进而展现出一种温和修复
查看详情
最近由国家药品监督管理局公布的一项正式批准三款创新医疗器械产品上市注册申请的重要消息中,涉及来自国内多家医疗科技企业的产品,慧扬医疗科技(苏州)有限公司的射频穿刺
查看详情
关于医疗器械技术审评中心第六批外聘专家候选人的公示 为保障医疗器械技术审评工作科学公正,充分发挥外聘专家在医疗器械技术审评中的作用,根据《医疗器械技术审评中心
查看详情
根据《医疗器械注册与备案管理办法》《体外诊断试剂注册与备案管理办法》等相关规定,现将2025年12月贵州省药品监督管理局批准境内第二类医疗器械及体外诊断试剂有关情况
查看详情
根据《医疗器械标准管理办法》《医疗器械标准制修订工作管理规范》要求,国家药监局组织开展2026年医疗器械行业标准制修订项目遴选工作,经公开征求意见和组织专家论证,确定
查看详情
2025年12月,河北省药品监督管理局共批准首次注册第二类医疗器械产品32个(详见附件)。 特此公告。 附件:2025年12月批准首次注册第二类医疗器械产品目录 河北省药
查看详情
2025年12月,上海市药品监督管理局共批准首次注册医疗器械产品69项(具体产品见附件)。 特此通告。 附件:2025年12月批准注册医疗器械产品目录 上海市药品监督管理
查看详情
根据《医疗器械监督管理条例》相关规定,现将2025年12月广西药监局审批的第二类医疗器械产品注册信息予以公布。 2025年12月第二类医疗器械产品注册信息
查看详情