24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
2026年1月,国家药监局共批准注册医疗器械产品292个。其中,境内第三类医疗器械产品251个,进口第三类医疗器械产品23个,进口第二类医疗器械产品15个,港澳台医疗器械产品3个(具
查看详情
2026年最新版医用电气设备标准清单 序号 标准编号 标准名称 代替标准号 采标号 发布日期 实施日期
查看详情
2025年发布的医疗器械行业标准修改单清单 序号 标准编号 标准名称 发布日期 实施日期 归口单位 发布公告
查看详情
2025年发布的医疗器械行业标准清单 序号 标准编号 标准名称 发布日期 实施日期 归口单位 发布公告
查看详情
2025年发布的医疗器械国家标准清单 序号 标准编号 标准名称 发布日期 实施日期 归口单位 发布公告
查看详情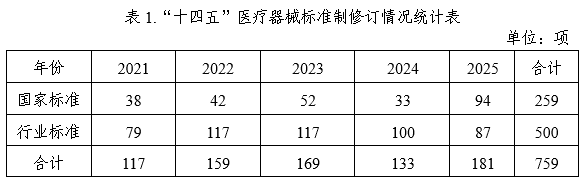
2025年,国家药监局坚持以习近平新时代中国特色社会主义思想为指导,全面贯彻落实党的二十大和二十届历次全会精神,以“四个最严”为根本遵循,按照“讲政治、
查看详情
2026年1月,河南省药品监督管理局共批准注册第二类医疗器械产品63个,具体产品详见附件。 特此公告。 附件:2026年1月批准注册医疗器械产品目录 2026年2月10日2026
查看详情
2026年1月进口第一类医疗器械产品备案信息 序号 产品名称 备案号 备案人名称原文 生产地址原文 备案日期 状态 1 高速台式冷冻离心
查看详情