24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
曾经在市场中一度备受各界热切追捧的中药注射剂,当前正处于一场被认为是前所未有的监管风暴之下,就在10月9日这个特定日子里,由国家药监局、国家卫健委以及国家中医药局这三个部门联合对外发布相关公告《国家药监局 国家卫生健康委 国家中医药局关于进一步推进药品上市许可持有人加快开展中药注射剂上市后研究和评价工作的公告(征求意见稿)》,进一步积极推进中药注射剂的上市之后的研究以及评价等方面的工作,而这一举动在业内往往被视作关系着中药注射剂未来生存与否的所谓“生死劫”。
政策背景:三部门联合出手,中药注射剂监管趋严
在经历较为漫长的一段时期以内,一直处在争议所形成的如同漩涡一般态势之中的中药注射剂,此次因三部门以联合的方式所发布的公告,使得可被视作标志着这样一种状况,那便是国家针对于中药注射剂所施行的管理行为,即将要以动“真刀子”的这种方式被展现出来。
这项目前直接影响所有中药注射剂品种未来命运的政策,致使按规定中药注射剂持有人必须开展的上市后研究与评价工作,需证明产品安全性与有效性这一情况出现。
当这一涉及中药注射剂领域的政策得以出台之后,在业内引起了快速的反应,那些手中握着中药注射剂相关业务的企业,基于自身发展需求纷纷急切地找寻能实现业务持续或转型的出路,并且,伴随着这种情况的发生,中药CRO公司的问询电话也开始以较为频繁的状态不断响起,也正是因为这些一系列情况的出现,使得整个原本相对稳定的中药注射剂市场逐渐迎来重大且复杂的变局走向。
三类中药注射剂首当其冲
基药与医保目录内品种:优先开展评价
|
药品名称 |
医院全终端市场(亿元) |
持有人数量 |
|---|---|---|
|
注射用血塞通(冻干) |
36.03 |
2 |
|
丹参注射液 |
22.04 |
41 |
|
注射用血栓通(冻干) |
16.64 |
1 |
|
清开灵注射液 |
12.36 |
10 |
|
参麦注射液 |
11.13 |
8 |
|
血塞通注射液 |
3.48 |
16 |
|
生脉注射液 |
2.40 |
8 |
|
脉络宁注射液 |
1.25 |
1 |
|
柴胡注射液 |
0.57 |
73 |
|
血栓通注射液 |
0.56 |
4 |
被公告以明确要求“优先开展上市后研究和评价”所针对的品种,乃是处于基药范畴以及医保目录之内的那些,而据相关统计所示,在2024年医保目录之中存在着共计58个中药注射剂,其中竟然还有10个品种同时出现在基药目录与医保目录当中的这一情况。
那同时进入两大目录且临床使用量颇为巨大的10个品种,因其所具备的这些特性,将会被当作首批需要针对其开展详尽研究工作的重要对象,而基于它们在进入目录以及临床使用量方面呈现出的状况,也自然而然地使得它们成为被监管领域重点关注的核心对象所在之处。
销售额巨大的大品种:监管风暴核心
对于那些销售额呈现越高态势的品种而言,其往往面临着越大程度的监管压力这一状况,从相关数据中能够看出,在2024年这个特定年份里,中药注射剂于医院端所获得的销售额竟然达到了443亿元之多,而其中市场规模超出1亿以上的品种,总计数量为50个的这般情况。
超10亿市场规模的品种共计14个,其中只有五个是基药。这些大品种包括:
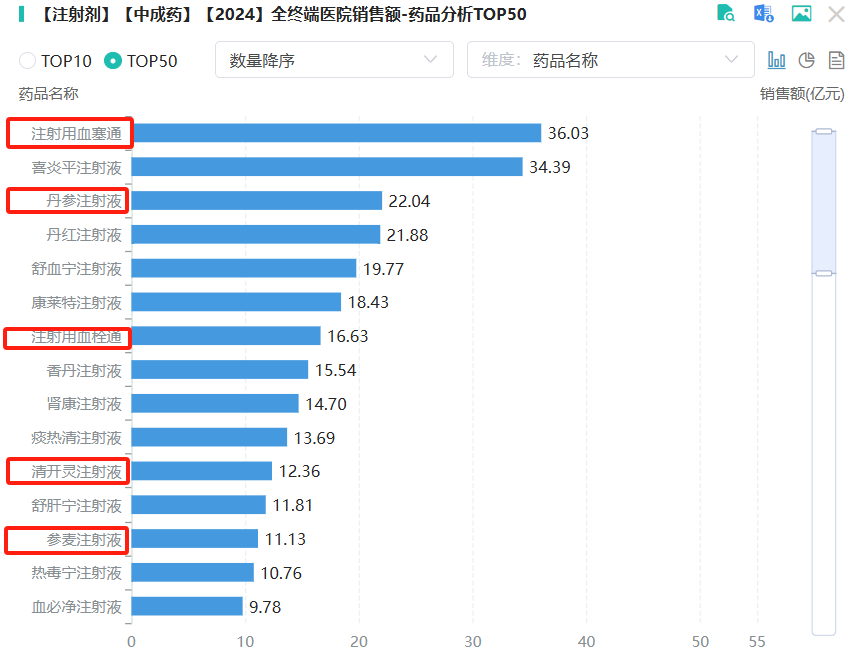
在药品市场领域之中存在着这样一种情况,即市场规模超过36亿的注射用血塞通,其持有人仅仅只有两家,这两家分别为哈尔滨珍宝制药以及昆药集团,而在整个市场份额的占据方面,二者处于基本将市场平分这样一种状态。
那被江西青峰药业作为独家品种拥有的喜炎平注射液,在过去长达十年的时间里所获取的销售额总计超出300亿之巨,虽说它的知名度是达到了甚广之程度,然而,与之如影随形般伴随的争议同样也是大到不容忽视。
丹参注射液:市场20亿+,有40多家企业竞争,市占率第一的是朗致集团万荣药业;
丹红注射液:山东丹红制药独家品种,2016年销售额达60亿以上,2024年仍有超20亿。
对于这些头部品种而言,上市后研究与再评价并非选择,而是生存门槛。
僵尸批文:无路可退的困境
第三类所涉及到的受影响对象呢,是那种长时间都处于未开展生产状态的所谓“僵尸批文”,而意见稿以一种明确指出的方式表明,对于那些长期处于未生产情况的品种而言,只有当持有人成功完成上市之后的研究以及评价这一系列活动,并且该品种在经过严格的审评之后,被判定为其所带来的获益在整体考量下要大于潜在风险的这一情形下,这个品种才能够按照规定恢复到上市销售的相关流程之中。
目前所呈现出的状况乃是,在众多的中药注射剂相关情况里,有效品种总计达135个之多,此情形涉及到数量为210家的药企以及900多个文号,然而实际处于销售状态的却仅仅只有93个品种以及142家企业,这样的现实情况无疑意味着至少有40个品种已然长期处于停产的局面,并且这种停产的状况还波及到70余家企业。
于 2026 年 3 月 1 日即将正式予以执行的那部被称之为《中药生产监督管理专门规定》的文件,以一种再次进行明确的方式指出,当中药注射剂欲恢复生产之时,就必须要完成那具有特定意义的上市之后的研究以及评价这一系列工作,而且还要同时提出相关的补充申请,然而在此过程之中,那两份文件几乎是以同步推进的形式,意在对僵尸批文进行彻底清理这般复杂且关联的事项。
企业应对策略与CRO市场机遇
当处在面对十分紧迫的那种时间要求情形之下时,企业必须依据自身所涉及到的品种具体情况来进行相应策略的制定工作,然而对于那些自始至终都一直在市场上进行销售的品种而言,其面临的主要难度却在于要去开展那具有一定挑战性的上市之后的临床安全性以及有效性方面的评价研究工作。
然而对于处于停产状态下的中药注射剂而言,所面临的困难点因其需要展开药学研究这一包括原辅料、包材、工艺、质量以及稳定性等众多方面的研究工作,并且还得进行非临床安全性研究涵盖药理学、毒理学以及安全性试验等相关内容,同时临床安全性有效性研究也不可或缺,故而显得更为复杂。
在这样一种特定的行业发展背景之下,去寻觅那些能够提供可靠服务的CRO并获得其大力协助,就已然成为了一种被众多相关主体所认为的具有高度合理性与优越性的最佳选择,尤为值得关注的是,在那些形形色色的CRO公司之中,能够顺利开展中药制剂临床试验项目的此类CRO公司,无疑将会迎接业务出现增长态势的良好机会。而当前的CRO行业,竞争呈现出极为激烈的状态,比如一款化药注射液开展一致性评价工作的报价,已然被压低至两百万金额界限以内,与此同时,中药注射剂新颁布的相关规定,注定会为那些在专业领域有所建树的CRO公司开辟出崭新的市场运作空间。
行业影响与未来展望
此次中药注射剂监管新政的实施,将对医药行业产生深远影响:
由于市场集中度呈现出不断提升的态势,那些因自身实力匮乏从而难以顺利完成研究评价工作的小企业,将会在这种环境下被迫无奈地选择退出市场,而与之相对的是,具备较强实力的龙头企业,其于市场之中所占据的份额将会得到进一步的扩大。
经由全面且严格至极的针对产品各方面细节进行的深度研究与综合评价之后,那部分最终能够成功留存于复杂多样充满竞争的市场之中的中药注射剂,必然将会具备在安全性以及有效性层面上更加坚实稳固的有力保障;而之所以会呈现这般状况,乃是基于多方因素相互作用且综合影响所致的,这些因素交织在一起,从不同角度对中药注射剂留存市场以及相应保障产生着意义深远且难以忽视的作用,进而才使得能留存市场的中药注射剂拥有如此特性。
在行业朝着规范化发展的进程之中,通过各式各样不同方式来促使行业实现从侧重于产品销售这样一种模式朝着着重进行研发的方向实现转变,进而在这一转变达成的基础之上对于中药注射剂的高质量发展起到有力的推动作用。
中药注射剂这一作为中医药现代化过程中所产生的极为重要成果的存在,其规范化地予以发展这一关键要点,事实上对于中医药事业在未来的长远走向而言,是有着紧密且不可忽视的关联的。而此次针对中药注射剂行业所推行的监管政策得以加强这一举措,倘若从短期的时间维度上去加以审视的话,就会给相关的各类企业带来程度各异的压力,然而一旦将视角切换至长期的时间范畴来进行考量,那必然是会有利于该行业达成健康且有序发展这一目标的。
随着那在2026年3月1日即将来临之际的《中药生产监督管理专门规定》正式实施日愈发临近之时,中药注射剂市场被推动着将会迎来那新一轮的市场格局变动情形,而只有那些真正能够经得起严谨科学评价这般考验的产品,才有可能最终以留存的状态停留在市场之上。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。