24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
为便于医疗器械行业从业者、监管机构及研究人员精准把握市场动态与合规要求,本文系统梳理了截至2025年中国大陆各省市及港澳台地区官方医疗器械注册信息查询途径。受分级
查看详情
2025年9月进口第一类医疗器械产品备案信息 序号 产品名称 备案号 备案人名称原文 生产地址原文 备案日期 状态 1 高分子固定绷带
查看详情
2025年9月,河南省药品监督管理局共批准注册第二类医疗器械产品147个,具体产品详见附件。 特此公告。 附件:2025年9月批准注册医疗器械产品目录 2025年10月11日202
查看详情
2025年9月,北京市药品监督管理局共批准注册第二类医疗器械产品29个(具体产品见附件)。 特此公告。 附件:2025年9月批准注册第二类医疗器械产品目录 北京市药品监
查看详情
2025年9月,各地市第一类医疗器械产品备案公告情况如下:济南: 序号 企业名称 业务名称 产品名称 备案号 1 山东志盈医学科技有限公司 第一类医疗器
查看详情
2025年9月,山东省药品监督管理局共批准注册第二类医疗器械产品52个(具体产品见附件)。 特此公告。 附件:2025年9月批准注册医疗器械产品目录.xlsx 山东省药品监
查看详情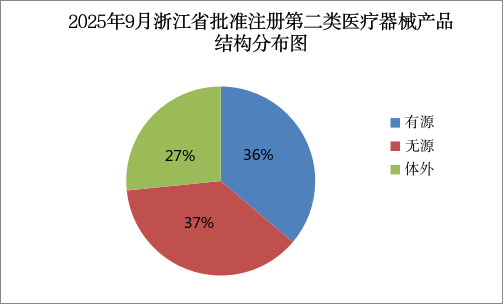
2025年9月,浙江省药品监督管理局共批准注册第二类医疗器械产品94个,其中有源类34个,无源类35个,体外诊断试剂25个(具体产品见附件)。 按照注册申请人所在辖区分析,批准注
查看详情
为进一步贯彻落实好《药品管理法》和《国务院办公厅关于全面深化药品医疗器械监管改革 促进医药产业高质量发展的意见》(国办发〔2024〕53号)、《国务院办公厅关于提升
查看详情