24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
2019年4月1日实施的认证模式新规定要求风险A类医疗器械获得医疗器械通知证书(CMDN),风险B,CD类医疗器械取得医疗器械注册证(CMDR)只有这样,我们才能在菲律宾进口并投放市场。研究临床试验展品捐赠及/或新的审计过程注意事项1.只有获得营业执照(LTO)只有当地机构才能在菲律宾注册医疗器械。3.质量体系资格评定B,C和D类设备ISO13485或FDA或日本PMDA审计报告。

为了提供岛国所需的全方位商品,菲律宾医疗保健行业严重依赖国外医疗器械和体外诊断设备制造商的进口。作为一个发展中的市场,对医疗器械的需求可以归因于6%的稳定经济增长和医院的持续扩张。
主管部门和核心法规
菲律宾的医疗器械注册由卫生部的设备、辐射健康和研究所控制(CDRRHR)管理。共和国法律和2009年《食品和药品管理法》对医疗器械进行了监管。
为了根据东盟医疗器械指令协调菲律宾控制指南,菲律宾卫生部发布了2018-0002号行政命令。行政命令引入了医疗器械的风险分类,以及对初始器械注册和更新的新要求。
产品类别
DOH行政令第2018-0002号题为“根据东盟协调技术要求签发医疗器械授权的指导方针”(指南),根据医疗器械的风险等级,对医疗器械实行分类制度,具体规定如下:
|
分类 |
风险等级 |
|
A |
低 |
|
B |
中低 |
|
C |
中高 |
|
D |
高 |
每一种分类的医疗器械清单应由PFDA发布指导文件。
在菲律宾,治疗或医疗用途的器械、机器、体外试剂、软件和类似或相关物品被视为医疗器械。根据东盟医疗器械的指示,菲律宾的原始产品类别统一分为A,B,C,D从低风险到高风险险到高风险分类。
IVD分类
IVD与其它医疗器械分类,按风险由低到高,分为:A级,B类,C类,D类。风险取决于预期用途、预期客户的专业知识、诊断结果信息的重要性以及测试结果的影响。比如怀孕测试是B级,而怀孕测试是B级,HIVD级血液检测。
认证模式
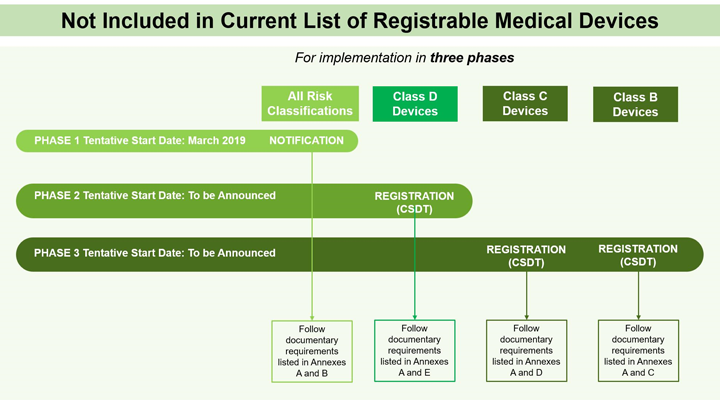
2019年4月1日实施的新规定要求风险A类医疗器械获得医疗器械通知证书(CMDN),风险B,CD类医疗器械取得医疗器械注册证(CMDR)只有这样,我们才能在菲律宾进口并投放市场。新规定将分阶段实施:
1.A类医疗器械都必须有CMDN,2021-0021-001)-A)B,C必须有D类医疗器械CMDR。
未通知(未通知)-A在B,C和D类医疗器械必须在2023年4月1日前开始CMDN,之后,更新需要涉及更多CMDR。
所有类别的设备都应由国家或参照国家许可。参考国家包括澳大利亚、加拿大、欧盟、日本、美国等。以下类别的一些医疗设备可以免除CMDN或CMDR,但是仍然需要医疗器械清单:
研究
临床试验
展品
捐赠和/或新颖
审核流程
1.注意事项
1.只有获得营业执照(LTO)
只有当地机构才能在菲律宾注册医疗设备。当地医疗设备买家、分销商(买家、出口商和批发商)、贸易商和制造商受到影响CDRRHR的LTO约束。
2.除原籍国/参照国的许可外
通知和注册也应符合要求CSDT技术文件模板。通知需要设备描述、符合性证书、符合性声明、保质期声明和清晰、完整、彩色标签图片。
3.质量体系资格评定
B,C和D类设备ISO13485或FDA或日本PMDA审计报告,以确认合法或实际制造设施的质量体系。
4.注册必要的文件
授权委托书(授权委托书副本应附有法律制造商或产品所有权真实性的公证声明原件)。
政府颁发的证书证明制造商在人员和设施方面的能力和可靠性、质量体系许可证或许可证ISO13485合规证书(证书副本应附有法律制造商或产品所有者的公证声明副本,以确认证书的真实性和正确性。
由原产国监管部门或批准的公告机构颁发的产品注册证书或任何等效文件,以确认设备的安全性和有效性(证书副本应附有法律制造商或产品所有者确认证书真实性的公证声明原件)
5.有效期和续证
CMDN和CMDR有效期为5年,初始批准后必须每五年更新一次。CMDR或CMDN提交续签到期前90天。
根据旧规则颁发的产品注册证书(CPR)它将一直有效,直到到期,许可证更新申请将生成一个新的CMDN,菲律宾比索(110美元)有效期为5年,费用为5150美元。根据旧规则颁发的豁免证书(COE)有效期为2021年11月3日,或签发后两年(以较短者为准)。
6.许可证转让
对于CMDN/CMDR对于转让项目,飞速度将要求审查当前许可证和综合外国代理协议的副本。转让申请应提供注册证明原件。飞速度将帮助从目前在菲律宾的持有人处获得该文件。
7.许可证持有人(持有人)要求
许可证持有人必须参与其持有进口许可证的设备的清关流程。竞争性招标第三方服务(如货运代理)按转让方式收费。每个事件都将生成一份运输报告,以记录费用和文件收据。买方、分销商或制造商的营业执照必须通过外国制造源数据进行更新。
8.使用飞速度作为您的独立许可持有人的优势
直接销售给多个区域经销商,防止国家买家涨价
提高转让定价
提高经销商谈判/响应的杠杆效应
根据需要添加或更改分销商
让知识产权远离当地的商业代理
确保专家处理上市后的警惕性和许可证维护
9.菲律宾无线医疗器械注册
在菲律宾,选择无线技术(例如蜂窝,RFID,WiFi或蓝牙)医疗设备被视为无线电通信设备(RCE),并接受国家电信委员会(NTC)限制监管要求。每种产品都必须经过设备型式的批准(DTA)证书,每件进口货物必须取得进口许可证。需要注意的是,即使主机医疗设备目前在菲律宾,FDA注册豁免(例如,未经通知的医疗设备),也要遵守这些无线技术注册要求。
10.菲律宾的独立软件是否被视为医疗器械?
菲律宾新的医疗器械法规(参考第2018-0002号行政命令)明确规定,软件包含在医疗器械的定义中(参考第15节医疗器械第4条)。因此,有必要确定软件的预期用途是否符合医疗器械的标准。例如,用于健康、生活习惯和健身的软件通常不被视为医疗设备。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。