24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

随着中国近视人群的增加,隐形眼镜的使用普及率也越来越高,同时也促进了隐形眼镜护理产业的发展。台湾的接触镜及其护理产品行业发达,占中国大陆市场份额相对较大,本文主要讨论台湾企业如何满足中国大陆法规对于接触镜护理产品上市要求。
根据《医疗器械分类目录》,接触镜护理产品的分类编码为16-06-02,属于第三类医疗器械管理,根据其功能的差异被细分为五大类。
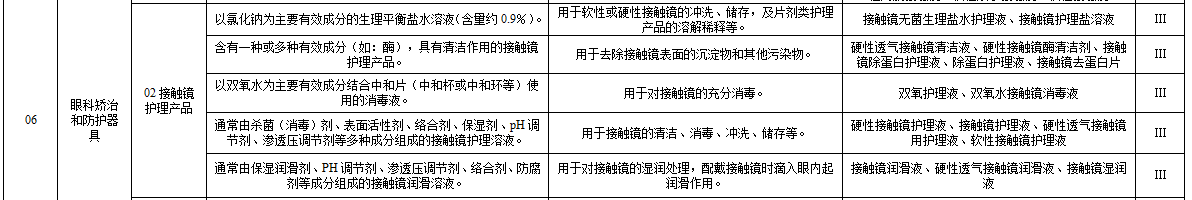
根据《免于进行临床评价医疗器械目录》,上述五种类型的接触镜护理产品只有盐溶液可豁免临床评价,其余功能的产品均需要进行临床评价。临床评价的方式有临床试验、同品种比对、使用境外临床试验数据、真实世界临床试验数据等途径,企业可根据已有的临床数据类型分析选择。

在制定产品技术要求时,应参考《YY 0719.2-2009 眼科光学 接触镜护理产品 第2部分:基本要求》进行制定,同时应对产品的外观、PH、渗透压、粘度、溶解时间、中和时间、装量、与接触镜的物理相容性、有效成分、过氧化氢残留量、清洁效率、微生物限度、抗微生物活性、防腐有效性及开瓶抛弃周期、有效期进行检测。检测方法参考《中国药典》及YY0719系列标准。其中有效成分、清洁效率的检测方法应由企业提供,若无标准检测方法的应提供方法学论证资料,目前EDTA、泊洛沙姆、环氧乙烯氢化蓖麻油成分的检测方法可参考YY0719.8 和YY0719.9。
接触镜护理产品应确定适用的接触镜的材料,应根据标准YY 0719.5进行镜片相容性试验,试验镜片应每组不少于10片并包含极端顶焦度。接触镜的材料组别详见GB/T11417.1(ISO 18369-1),但是硅水凝胶镜片建单独进行相容性试验。
接触镜护理产品的抗微生物活性、防腐有效性和开瓶抛弃周期可在有效期研究中进行验证,具体详见《台湾企业如何申报接触镜护理产品注册(二)》。
接触镜护理产品的生物相容性研究应包括细胞毒性、皮肤刺激、眼刺激、急性经口毒性。若采用新的眼用成分或不同的有效成分的产品(即国内已上市产品无该成分)还应进行皮肤致敏、兔眼相容性试验以及防腐剂的摄入和释放的测定。
接触镜护理产品的检测应注意典型性样品的选择可参考有效期研究中的典型性样品,送检样品需要准备三个批次(2:1:1比例准备),建议提前沟通送检规格及数量。防腐有效性研究根据防腐剂的种类、使用方法、适配的镜片种类等的差异,其试验样品数量可能存在差异,送检前应与试验机构充分沟通,并需要准备防腐剂的标准品或具有溯源信息的对照品。目前,较为推荐的接触镜护理产品的检验机构为浙江省医疗器械检验研究院。
台湾地区医疗器械企业可根据在台湾地区或其他国家上市时的已有资料评估上述研究项目是否需要重新开展。大陆的接触镜护理产品参考的标准等同于ISO标准,而台湾地区推行的接触镜护理产品标准也是参考ISO标准,故而基本可以直接采用已有的研究资料。而针对技术要求的检测报告也可提交在台湾地区或其他国家有资质的第三方出具的报告及资质证明,企业具有相应检验能力的也可以提交自检报告。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。